O 24 de marzo de 2026 celébrase o 31º Día Mundial da Tuberculose. A Organización Mundial da Saúde (OMS) anunciou o tema mundial deste ano como"Si! Podemos acabar coa tuberculose!", facendo fincapé en que un liderado gobernamental forte, un compromiso político sostido e unha acción multisectorial coordinada son esenciais para acabar coa epidemia de tuberculose (TB).

Progreso global e desafíos pendentes
Segundo o Informe mundial sobre a tuberculose de 2025, o control mundial da tuberculose alcanzou un fito significativo en 2024, tanto con...incidencia e mortalidade en descensopor primeira vez desde a pandemia da COVID-19.
Estímase que10,7 millóns de persoasdesenvolveron tuberculose en 2024, incluíndo o 54 % de homes, o 35 % de mulleres e o 11 % de nenos e adolescentes. Entre estes casos, aproximadamente619.000 (5,8 %)estaban coinfectados co VIH e390.000 (3,6 %)eran tuberculoses multirresistentes ou resistentes á rifampicina (TB-MDR/RR).
Tuberculose causada aproximadamente1,23 millóns de mortesen 2024, manténdose como a principal causa infecciosa de morte a nivel mundial, superando á COVID-19. Tras tres anos de aumentos entre 2021 e 2023, a incidencia mundial da tuberculose diminuíu case un 2 % en 2024, o que reflicte unha recuperación gradual dos servizos de atención á tuberculose.[1]
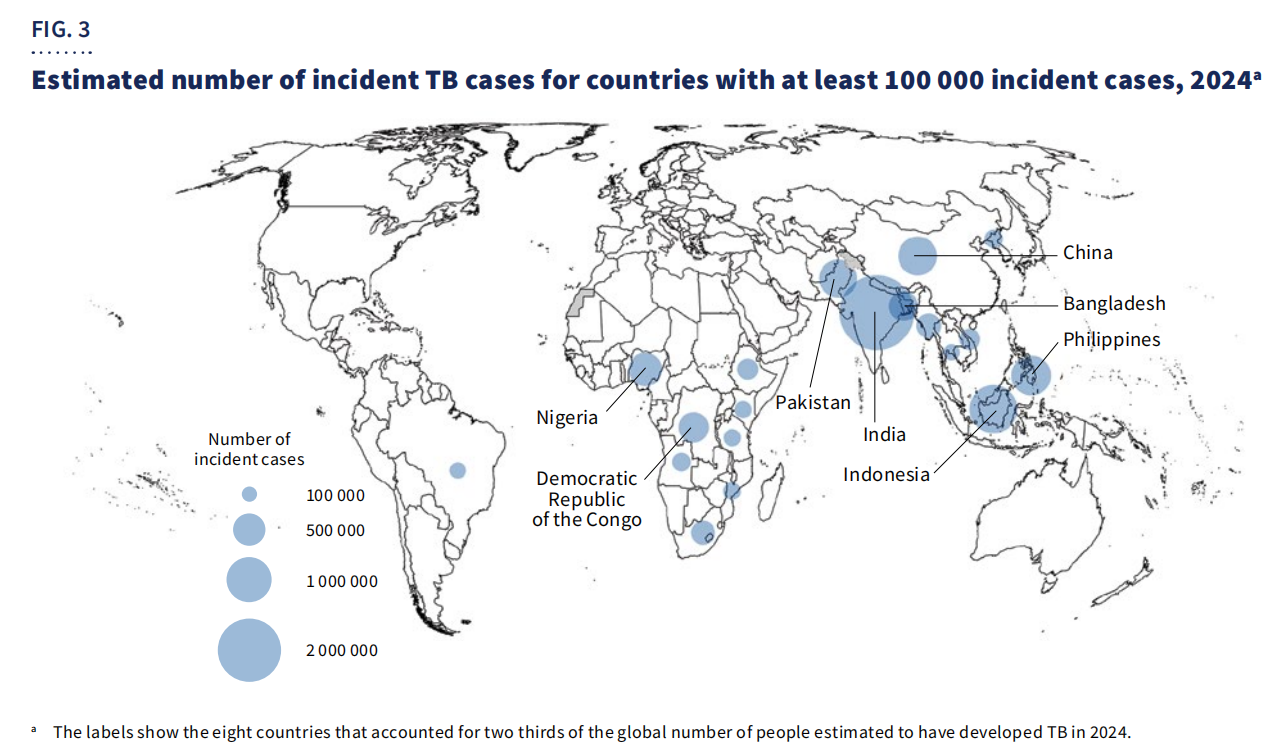
Xeograficamente,67 % dos casosconcentráronse en oito países: India, Indonesia, Filipinas, China, Paquistán, Nixeria, República Democrática do Congo e Bangladesh.
Malia os progresos, a tuberculose segue a ser unha das principais causas de morte entre as persoas que viven co VIH e un dos principais contribuíntes á mortalidade asociada á resistencia aos antimicrobianos. O financiamento global segue a ser insuficiente, con só5.900 millóns de dólares estadounidensesdispoñible en 2024, moi por debaixo doObxectivo anual de 22.000 millóns de dólares estadounidensesfixado para 2027.
Estas cifras salientan a necesidade urxente de fortalecer os programas de control da tuberculose a nivel mundial, centrándose en ampliar o acceso aos diagnósticos, mellorar os resultados do tratamento e abordar os determinantes sociais que impulsan a transmisión da tuberculose. A tuberculose segue a requirir unha sólida cooperación internacional e un compromiso político para cumprir os obxectivos da Estratexia para acabar coa tuberculose.
Mycobacterium tuberculosis: Patoxénese e clasificación
A Mycobacterium tuberculosis (MTB/M. tuberculosis) é o principal e máis común patóxeno responsable da tuberculose (TB). Pode entrar no corpo humano a través do tracto respiratorio, o tracto dixestivo ou a pel e as membranas mucosas danadas, infectando múltiples órganos e causando diferentes formas de tuberculose. A tuberculose pulmonar, transmitida principalmente a través de gotículas, representa máis do 80 % dos casos de tuberculose. Os síntomas comúns inclúen tose, produción de esputos e hemoptise. Despois da infección nos pulmóns, a bacteria pode propagarse a través da corrente sanguínea a múltiples sistemas, o que pode levar á tuberculose esquelética, urinaria ou gastrointestinal.[2]
A MTB forma parte do xénero Mycobacterium, que inclúe:
- Complexo Mycobacterium tuberculosis (MTBC): comprende M. tuberculosis, M. bovis, M. africanum, M. canettii e M. microti, entre outros. Aínda que M. tuberculosis é a principal causa da tuberculose, M. bovis e M. africanum tamén poden inducir a enfermidade.
- Micobacterias non tuberculosas (NTM).
- Mycobacterium leprae, a causante da lepra.
Enfoques de diagnóstico de laboratorio
Un diagnóstico preciso e oportuno é esencial para un control eficaz da tuberculose. A Organización Mundial da Saúde subliña queAs tecnoloxías de diagnóstico molecular rápido transformaron fundamentalmente a detección da tuberculose ao permitir a identificación altamente sensible e específica de patóxenos e, ao mesmo tempo, a detección da resistencia aos fármacos.[1].
- Microscopía e Cultivoe: O cultivo segue a ser o método de referencia para o diagnóstico da tuberculose, xa que permite a identificación definitiva de organismos viables e facilita as probas de sensibilidade aos fármacos e a análise xenómica. Non obstante, debido á lenta taxa de crecemento de Mycobacterium tuberculosis, os resultados adoitan requirir de 2 a 8 semanas, o que limita a súa utilidade clínica na toma de decisións urxentes.
-Probas inmunolóxicas: Os métodos inmunolóxicos, como a proba cutánea da tuberculina (TST) e os ensaios de liberación de interferón gamma (IGRA), detectan as respostas inmunitarias do hóspede á infección por tuberculose. Aínda que son útiles para identificar infeccións latentes, estes ensaios non poden distinguir de forma fiable entre a infección activa e a previa e, polo tanto, teñen unha especificidade diagnóstica limitada en contextos de alta carga.
-Diagnóstico Molecular (NAAT): Recoméndanse probas baseadas no ADN como a amplificación de ácidos nucleicos (NAAT) pola súa alta sensibilidade e especificidade.
-Secuenciación de nova xeración dirixida (tNGS): As tecnoloxías de secuenciación dirixida proporcionan unha identificación de alta resolución de mutacións asociadas á resistencia. As directrices da OMS recomendan a tNGS como unha ferramenta avanzada para a detección da resistencia a fármacos posdiagnóstico, o que apoia as estratexias de tratamento de precisión [3].
-Secuenciación metaxenómica de nova xeración (mNGS): A secuenciación metaxenómica permite a detección imparcial dunha ampla gama de patóxenos sen selección previa de dianas. Esta estratexia é especialmente valiosa en escenarios clínicos complexos ou pouco claros, como infeccións mixtas e pacientes inmunodeprimidos, onde os diagnósticos convencionais poden ser insuficientes.
A OMS destaca ademais que a confirmación microbiolóxica é esencial para iniciar unha terapia axeitada e mellorar os resultados dos pacientes, o que reforza a importancia de integrar o diagnóstico molecular avanzado nos programas de control da tuberculose [1].
Solucións completas de diagnóstico molecular de macro e micro probas
1.Detección por PCR múltiple para a tuberculose e a resistencia aos fármacosTuberculose
| Código do produto | Nome do produto | Certificación |
| HWTS-RT001 | Kit de detección de ADN de Mycobacterium Tuberculosis (PCR de fluorescencia) | CE |
| HWTS-RT137 | Kit de detección de mutacións de resistencia á isoniazida de Mycobacterium Tuberculosis (curva de fusión) | CE |
| HWTS-RT074 | Kit de detección de ácidos nucleicos e resistencia a rifampicina de Mycobacterium Tuberculosis (curva de fusión) | CE |
| HWTS-RT102 | Kit de detección de ácidos nucleicos baseado na amplificación isotérmica de sondas enzimáticas (EPIA) para Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Kit de detección de ácidos nucleicos do complexo Mycobacterium Tuberculosis liofilizado (amplificación isotérmica con sonda enzimática) | CE |
| HWTS-RT105 | Kit de detección de ADN de Mycobacterium Tuberculosis liofilizado (PCR de fluorescencia) | CE |
| HWTS-RT147 | Kit de detección de resistencia a isoniazida e rifampicina e ácido nucleico de Mycobacterium Tuberculosis (curva de fusión) | CE |
Cando existe unha forte sospeita clínica de tuberculose (TB), oHWTS-RT147Recoméndase a proba para a detección cualitativa da infección por MTB e da tuberculose multirresistente (TB-MDR). Esta proba identifica mutacións noxene rpoB, que provocan resistencia á rifampicina (RIF) e mutacións noXenes katG e InhA, que están asociados coa resistencia á isoniazida (INH). Ofrece unha proba eficiente e única tanto para a MTB como para a MDR-TB, e incorpora control de calidade interno para minimizar os resultados falsos negativos, garantindo resultados rápidos e precisos.
2.Secuenciación dirixida de PTNseq para patóxenos respiratorios e perfís de resistencia
| Código do produto | Nome do produto | Especificación |
| HWKF-TS0001 | Kit de enriquecemento xenético de patóxenos de infeccións sanguíneas PTNseq | 24 probas/kit |
| HWKF-TS0002 | Kit de enriquecemento xenético de microorganismos patóxenos para infeccións do sistema nervioso central PTNseq | 24 probas/kit |
| HWKF-TS0003 | Kit de enriquecemento xenético de patóxenos de infeccións respiratorias PTNseq | 24 probas/kit |
| HWKF-AT0003 | Kit de construción de bibliotecas de enriquecemento automatizado para microorganismos patóxenos de infeccións respiratorias PTNseq (ONT) | 24 probas/kit |
| HWKF-TS0004 | Kit de enriquecemento xenético de patóxenos infecciosos de amplo espectro PTNseq | 24 probas/kit |
| HWKF-TS0005 | Kit de enriquecemento xenético de microorganismos patóxenos infecciosos de espectro ultraamplio PTNseq | 24 probas/kit |
| HWKF-TS0151 | Kit de tipificación de micobacterias e enriquecemento xénico de resistencia a fármacos (método de amplificación múltiple) | 24 probas/kit |
En casos de infeccións respiratorias mixtas (incluíndo infeccións das vías respiratorias superiores e inferiores, tuberculose e enfermidades respiratorias crónicas) ou cando se require unha análise de xenes de resistencia a fármacos (por exemplo, sospeita de tuberculose resistente a fármacos), oSerie PTNseq de detección de xenes de alto rendemento dirixidapódese aplicar. Baseado na tecnoloxía avanzada de secuenciación dirixida, PTNseq emprega a PCR ultramultiplex para enriquecer secuencias diana específicas, combinada coa secuenciación de alto rendemento e a tecnoloxía de nanoporos de terceira xeración para a identificación exhaustiva de patóxenos e a elaboración de perfís de resistencia a fármacos.
O sistema emprega cebadores patentados de alta especificidade para a amplificación ultramultiplex de xenes diana. Apoiado por unha base de datos patentada e algoritmos bioinformáticos intelixentes, proporciona unha identificación precisa de patóxenos xunto coa análise de xenes de resistencia a fármacos e virulencia. O enriquecemento dirixido reduce a interferencia do ADN hóspede, mellorando a sensibilidade en mostras con altos niveis de antecedentes humanos e permitindo a detección eficaz de dianas difíciles comoMycobacterium tuberculosis, fungos, bacterias intracelulares, virus de ARN e xenes de resistencia ou virulencia.
PTNseq alcanza un límite de deteccióntan baixo como 100 copias/mle cubertas175 patóxenos respiratorios comúns, incluíndo 76 bacterias, 73 virus, 19 fungos, 7 micoplasmas, así comoClamidia, Rickettsiae 54 xenes de resistencia a fármacosO panel inclúe oMycobacterium tuberculosisMicobacterias non tuberculosas complexas e importantes.
A serie PTNseq combina unha alta sensibilidade coa rendibilidade, mellorando as taxas de detección de patóxenos e apoiando a terapia antimicrobiana individualizada, á vez que axuda a mitigar a resistencia antimicrobiana. Integrada co sistema de preparación de bibliotecas de secuenciación de xenes (AIOS) totalmente automatizado, proporciona unha solución hospitalaria optimizada cun tempo de resposta de tan só 6,5 horas desde a mostra ata o resultado.

3. Secuenciación metaxenómica para a detección de patóxenos de amplo espectro
| Código do produto | Nome do produto | Especificación |
| HWKF-MN0011 | Kit de detección de patóxenos metaxenómicos (DNA-Illumina) | 24 probas/kit |
| HWKF-MN0018 | Kit de detección de patóxenos metaxenómicos (DNA-MGI) | 24 probas/kit |
| HWKF-MN0021 | Kit de detección de patóxenos metaxenómicos (DNA-ONT) | 24 probas/kit |
| HWKF-MN0012 | Kit de detección de patóxenos metaxenómicos (RNA-Illumina) | 24 probas/kit |
| HWKF-MN0019 | Kit de detección de patóxenos metaxenómicos (ARN-MGI) | 24 probas/kit |
| HWKF-MN0022 | Kit de detección de patóxenos metaxenómicos (RNA-ONT) | 24 probas/kit |
| HWKF-MN0013 | Kit de detección de patóxenos metaxenómicos (ADN+ARN-Illumina) | 24 probas/kit |
| HWKF-AYM0013 | Kit de construción automatizada de bibliotecas para a detección metaxenómica de patóxenos (ADN+ARN-Illumina) | 24 probas/kit |
| HWKF-MN0020 | Kit de detección de patóxenos metaxenómicos (ADN+ARN-MGI) | 24 probas/kit |
| HWKF-MN0023 | Kit de detección de patóxenos metaxenómicos (ADN+ARN-ONT) | 24 probas/kit |
Cando o diagnóstico clínico non é claro,Detección de xenes de alto rendemento de patóxenos mNGSpódese realizar en varias mostras do paciente, incluíndo líquido de lavado broncoalveolar, esputo, frotis de gorxa, sangue, derrame pleural, pus e mostras de tecido. Esta abordaxe emprega tecnoloxía de secuenciación metaxenómica, onde diferentes mostras se someten a un pretratamento específico seguido dunha extracción de ácidos nucleicos mediante esferas de vidro e encimas dixestivas da parede, o que mellora a eficiencia da extracción. A secuenciación adáptase a múltiples plataformas, o que garante un alto volume de datos para mellorar a sensibilidade da mNGS e a integridade do ensamblaxe. Os datos analízanse mediante unha base de datos autoconstruída e algoritmos intelixentes para detectarmáis de 20.000 patóxenos, incluíndo bacterias, fungos, virus e parasitos, proporcionando información sobre microorganismos patóxenos sospeitosos. Este método é axeitado para pacientes de difícil diagnóstico, en estado crítico ou inmunodeprimidos, incluíndo a identificación deBTTcomplexoeNTM, así como infeccións mixtas. Mellora significativamente as taxas de detección de patóxenos e axuda a guiar o uso clínico específico de antibióticos, o que permite un diagnóstico preciso da infección.
Conclusión
Aínda que se acadaron avances substanciais, a tuberculose segue a ser un importante desafío para a saúde mundial, especialmente no contexto da resistencia aos medicamentos, as carencias de financiamento e o acceso desigual aos diagnósticos.
A OMS subliña que ampliar o acceso a diagnósticos moleculares rápidos e tecnoloxías de secuenciación avanzadas é esencial para acadar os obxectivos da Estratexia para acabar coa tuberculose. Coa innovación, o investimento e a colaboración mundial continuos, acabar coa tuberculose xa non é unha aspiración, senón un obxectivo alcanzable.
Referencias:
- Organización Mundial da Saúde. Informe sobre a tuberculose mundial 2024/2025: probas diagnósticas e tratamento.
- Organización Mundial da Saúde. Manual da OMS para a selección de probas de diagnóstico rápido moleculares recomendadas pola OMS para a detección da tuberculose e da tuberculose farmacorresistente.
- Organización Mundial da Saúde. Directrices consolidadas da OMS sobre a tuberculose: módulo 3: diagnóstico (actualización de 2024).
Data de publicación: 24 de marzo de 2026
