I. Visión xeral doESMODirectriz de 2025
En agosto de 2025, a ESMO publicou oficialmente a Guía de práctica clínica da ESMO para o diagnóstico, o tratamento e o seguimento do cancro de pulmón non microcítico en fase inicial e localmente avanzado, publicada na revista de oncoloxía Annals of Oncology. Trátase da primeira actualización completa desde a versión de 2017 e constitúe unha referencia moi autorizada para os oncólogos de todo o mundo.

O cancro de pulmón ten a maior incidencia e mortalidade de todas as neoplasias malignas a nivel mundial. Cada ano, hai máis de 2,2 millóns de casos novos e máis de 1,8 millóns de mortes, o que converte o cancro de pulmón na principal causa de morte relacionada co cancro tanto en homes como en mulleres. O cancro de pulmón non microcítico (NSCLC) representa aproximadamente o 80-85 % de todos os pacientes con cancro de pulmón. Neste grave contexto, a publicación da guía de 2025 inxecta un novo impulso científico na práctica clínica, sendo especialmente crítica a actualización das estratexias de probas de biomarcadores.
II. Interpretación das actualizacións clave das directrices
2.1 Probas de biomarcadores: de "opcional" a "esencial"
A guía de 2025 introduce un axuste estratéxico fundamental en canto ás probas de biomarcadores. A guía afirma explicitamente que as probas de biomarcadores son esenciais para a toma de decisións terapéuticas en pacientes con NSCLC en estadio IB-III.
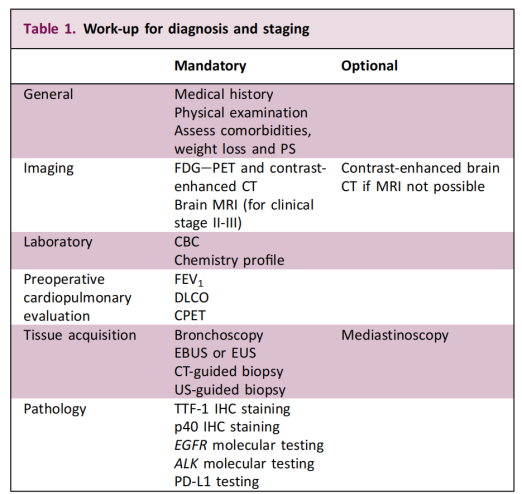
Esta recomendación amplía as probas moleculares desde o seu enfoque anterior en pacientes con enfermidade avanzada a casos resecables en estadios temperáns. O obxectivo principal é identificar as mutacións dos xenes impulsores e proporcionar unha base científica para un tratamento de precisión personalizado. A guía tamén subliña que a viabilidade da biopsia e o enfoque diagnóstico deben ser determinados por un equipo multidisciplinar en función das características do paciente e do tumor.
En canto á estratexia específica de probas, a guía recomenda claramente que as probas xenéticas se realicen antes da toma de decisións cirúrxicas e que, como mínimo, deberían abarcar EGFR e ALK. Este concepto de "probas anticipadas" ten unha profunda importancia clínica para a estratificación precisa e o tratamento personalizado do NSCLC en estadio inicial: a puntualidade e a precisión dos resultados das probas determinan directamente a elección da terapia adxuvante posterior.
2.2 Avances terapéuticos no NSCLC en estadio inicial positivo para o oncoxene do condutor
A guía de 2025 integra evidencias de múltiples estudos clínicos importantes para establecer unha vía de tratamento de precisión clara para pacientes con NSCLC en estadio inicial positivo para o oncoxene do condutor.
Pacientes con mutación positiva para o EGFR:Baseándose no ensaio histórico ADAURA, o osimertinib adxuvante posoperatorio durante tres anos converteuse no tratamento estándar global para pacientes con delecións do exón 19 do EGFR ou mutacións L858R do exón 21. O ensaio ADAURA é un estudo internacional, multicéntrico, aleatorizado e controlado de fase III que avalía a eficacia e a seguridade do osimertinib adxuvante en pacientes con NSCLC con mutación do EGFR en estadio IB-IIIA completamente resecado. O estudo mostrou que o osimertinib mellorou significativamente tanto a supervivencia libre de enfermidade como a supervivencia global en comparación co placebo, o que establece o osimertinib como o novo tratamento estándar para esta poboación. Non obstante, as análises exploratorias do ensaio ADAURA indicaron que aproximadamente o 36 % das interrupcións temperás do tratamento foron causadas por eventos adversos e outro 31 % por decisión do paciente. Este achado destaca a necesidade de realizar probas basais precisas antes do tratamento para garantir que se administre unha terapia dirixida aos pacientes que poidan obter un beneficio sostido.
Pacientes ALK positivos:Segundo o ensaio ALINA, o alectinib adxuvante posoperatorio durante dous anos é agora o tratamento estándar. Na análise primaria do ensaio ALINA aleatorio e aberto de fase III, o alectinib mostrou un beneficio notable na supervivencia libre de enfermidade na poboación en estadio II-IIIA, cunha razón de risco de 0,24. Os datos actualizados do ensaio ALINA presentados no congreso ESMO 2025 mostraron que, despois de ≥3 anos de seguimento, o beneficio da supervivencia libre de enfermidade do alectinib mantívose "sostido e clinicamente significativo", cunha razón de risco de 0,36 na poboación en estadio II-IIIA. A última taxa de supervivencia global a 4 anos notificada alcanzou o 98,4 %, a taxa de supervivencia libre de enfermidade a 4 anos foi do 75,5 % e a supervivencia libre de enfermidade do sistema nervioso central tamén mellorou, sen novos sinais de seguridade. Estes datos sólidos establecen aínda máis o alectinib adxuvante como o tratamento estándar despois da resección do NSCLC ALK-positivo e subliñan o valor das probas precisas para identificar a estes pacientes.
Escolla do método de proba:A guía da ESMO de 2025 enumera explicitamenteensaios de panel de RT-PCR multiplexxunto coa NGS baseada en ARN, a IHC e a FISH como unha das abordaxes técnicas recomendadas para a detección da fusión de ALK. Isto indica que o requisito principal da guía é realizar probas para guiar as decisións clínicas, en lugar de esixir unha plataforma de probas específica. Para os produtos de RT-PCR centrados na detección de EGFR e ALK, esta estratexia de probas flexible proporciona unha sólida xustificación baseada en guías para o seu uso na práctica clínica.
III. Solucións técnicas de probas de precisión
A guía de 2025 adianta as probas á fase de toma de decisións precirúrxicas, o que eleva o listón da precisión, a sensibilidade e a accesibilidade dos ensaios. Os dous produtos de detección baseados en RT-PCR que se describen a continuación aliñanse precisamente cos requisitos da guía desde unha perspectiva técnica.
Kit de detección de mutacións do EGFR 3.1: plataforma tecnolóxica ARMS mellorada
Tecnoloxía centralA tecnoloxía ARMS mellorada permite a amplificación específica de secuencias mutantes de baixa abundancia contra un fondo de tipo salvaxe elevado
Tres garantías técnicas:
-ARMS mellorado → mellora o recoñecemento de mutacións
-Enriquecemento encimático → dixire o fondo de tipo salvaxe e enriquece as secuencias mutantes
Bloqueo de temperatura → suprime a amplificación non específica
RendementoSensibilidade de1 % de frecuencia alélica mutante
Control da contaminaciónControl interno integrado + encima UNG que impiden a contaminación
Tempo de respostaFuncionamento de tubo pechado, aproximadamente120 minutos
Compatibilidade de mostras:Tecido/biopsia líquidamostras → aborda o requisito de "probas previas"
Cobertura:45 mutaciónsnos exóns 18-21 do EGFR, que coinciden con precisión coas rexións destacadas polas pautas (delecións do exón 19 e do exón 21 L858R)
Uso clínicoGuía directamente a terapia con TKI do EGFR
Kit de detección de fusión EML4-ALK 3.2 MMT: solución de detección de fusión baseada en ARN

-Plataforma tecnolóxicaRT-PCR baseada en ARN: ofrece vantaxes inherentes sobre os métodos baseados en ADN para a detección de fusión
-Vantaxe baseada no ARNDetecta directamente transcritos de fusión expresados, evitando eficazmente os falsos negativos
-Probas do estudoEn fusións de ALK de baixa abundancia, a RT-PCR é significativamente máis fiable que as probas baseadas en ADN
-SensibilidadeDetecta fusións de ata20 copias por reacción
-Cobertura de variantes: Cubertas12 variantes comúns de fusión EML4-ALK(incluíndo a variante 1 ~33%; variantes 3a/3b xuntas ~29%)
-Operación e control da contaminaciónTubo pechado, ~120 minutos; controis de proceso integrados + encima UNG que impiden resultados falsos
-Compatibilidade de instrumentosCompatible con varios instrumentos de PCR en tempo real
-Aliñamento de directricesMoi consistente coa guía da ESMO
IV. Coherencia entre os ensaios e as recomendacións da guía
Os dous produtos de detección son moi coherentes coa guía ESMO 2025 para o cancro de pulmón non microcítico precoz e localmente avanzado nas seguintes dimensións clave:
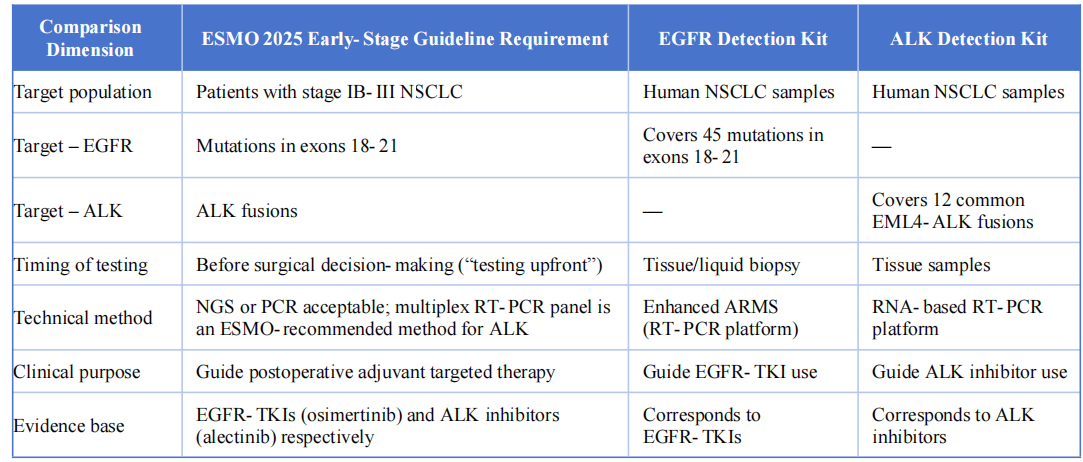
V. Conclusión
A guía ESMO 2025 para o NSCLC en estadio inicial marca o comezo dunha nova era de diagnóstico e tratamento de precisión, centrada en "probas previas, segmentación precisa e optimización do tratamento.O kit de detección de mutacións do EGFR e o kit de detección de fusión MMT EML4-ALK cumpren os requisitos da guía en canto a obxectivos, temporización e precisión a través de vías técnicas distintas.
O kit EGFR emprega tecnoloxía ARMS mellorada para a detección de alta sensibilidade de mutacións dirixidas en mostras limitadas, o que admite tanto biopsias de tecidos como líquidas para permitir a "realización de probas por adiantado".
O kit ALK baséase na RT-PCR baseada en ARN, o que ofrece vantaxes sobre os métodos de ADN para a detección de fusión, aliñándose coa recomendación da ESMO de paneis de RT-PCR multiplex para as probas de ALK.
Xuntos, estes dous produtos forman unha solución de probas de precisión que cumpre coa guía ESMO 2025, o que permite a terapia adxuvante personalizada para o NSCLC en estadio inicial.
Referencias:
- Zer A, Ahn MJ, Barlesi F, et al. Cancro de pulmón non microcítico precoz e localmente avanzado: Guía de práctica clínica da ESMO para o diagnóstico, tratamento e seguimento. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Data de publicación: 06-05-2026

