Resistencia a ácidos nucleicos e rifampicina de Mycobacterium Tuberculosis
Nome do produto
HWTS-RT074B-Kit de detección de ácidos nucleicos e resistencia a rifampicina de Mycobacterium Tuberculosis (curva de fusión)
Certificado
CE
Epidemioloxía
Mycobacterium tuberculosis, coñecida abreviadamente como bacilo da tuberculose (TB), é a bacteria patóxena que causa a tuberculose. Actualmente, os fármacos antituberculosos de primeira liña que se usan habitualmente inclúen a isoniazida, a rifampicina e o hexambutol, etc. Os fármacos antituberculosos de segunda liña inclúen as fluoroquinolonas, a amikacina e a kanamicina, etc. Os novos fármacos desenvolvidos son a linezolida, a bedaquilina e o delamani, etc. Non obstante, debido ao uso incorrecto dos fármacos antituberculosos e ás características da estrutura da parede celular de Mycobacterium tuberculosis, Mycobacterium tuberculosis desenvolve resistencia aos fármacos antituberculosos, o que supón serios desafíos para a prevención e o tratamento da tuberculose.
A rifampicina úsase amplamente no tratamento de pacientes con tuberculose pulmonar desde finais da década de 1970 e ten un efecto significativo. Foi a primeira opción para acurtar a quimioterapia dos pacientes con tuberculose pulmonar. A resistencia á rifampicina débese principalmente á mutación do xene rpoB. Aínda que constantemente aparecen novos fármacos antituberculosos e a eficacia clínica dos pacientes con tuberculose pulmonar tamén seguiu mellorando, aínda existe unha relativa escaseza de fármacos antituberculosos e o fenómeno do uso irracional de fármacos na clínica é relativamente alto. Obviamente, a Mycobacterium tuberculosis en pacientes con tuberculose pulmonar non se pode eliminar completamente de maneira oportuna, o que finalmente leva a diferentes graos de resistencia aos fármacos no corpo do paciente, prolonga o curso da enfermidade e aumenta o risco de morte do paciente.
Canle
| Canle | Canles e fluoróforos | Tampón de reacción A | Tampón de reacción B | Tampón de reacción C |
| Canle FAM | Reporteiro: FAM, Quencher: Ningún | rpoB 507-514 | rpoB 513-520 | 38KD e IS6110 |
| Canle CY5 | Reporteiro: CY5, Quencher: Ningún | rpoB 520-527 | rpoB 527-533 | / |
| Canle HEX (VIC) | Reporteiro: HEX (VIC), Quencher: Ningún | Control interno | Control interno | Control interno |
Parámetros técnicos
| Almacenamento | ≤-18 ℃ na escuridade |
| Vida útil | 12 meses |
| Tipo de mostra | Esputo |
| CV | ≤5,0% |
| Nivel de detalle | Mycobacterium tuberculosis 50 bacterias/ml tipo salvaxe resistente á rifampicina: 2x103bacterias/ml mutante homocigoto: 2x103bacterias/ml |
| Especificidade | Detecta a Mycobacterium tuberculosis de tipo salvaxe e os sitios de mutación doutros xenes de resistencia a fármacos como katG 315G>C\A, InhA-15C>T, e os resultados das probas non mostran resistencia á rifampicina, o que significa que non hai reactividade cruzada. |
| Instrumentos aplicables: | Sistemas de PCR en tempo real SLAN-96P Sistema de PCR en tempo real BioRad CFX96 Sistema de PCR en tempo real LightCycler480® |
Fluxo de traballo
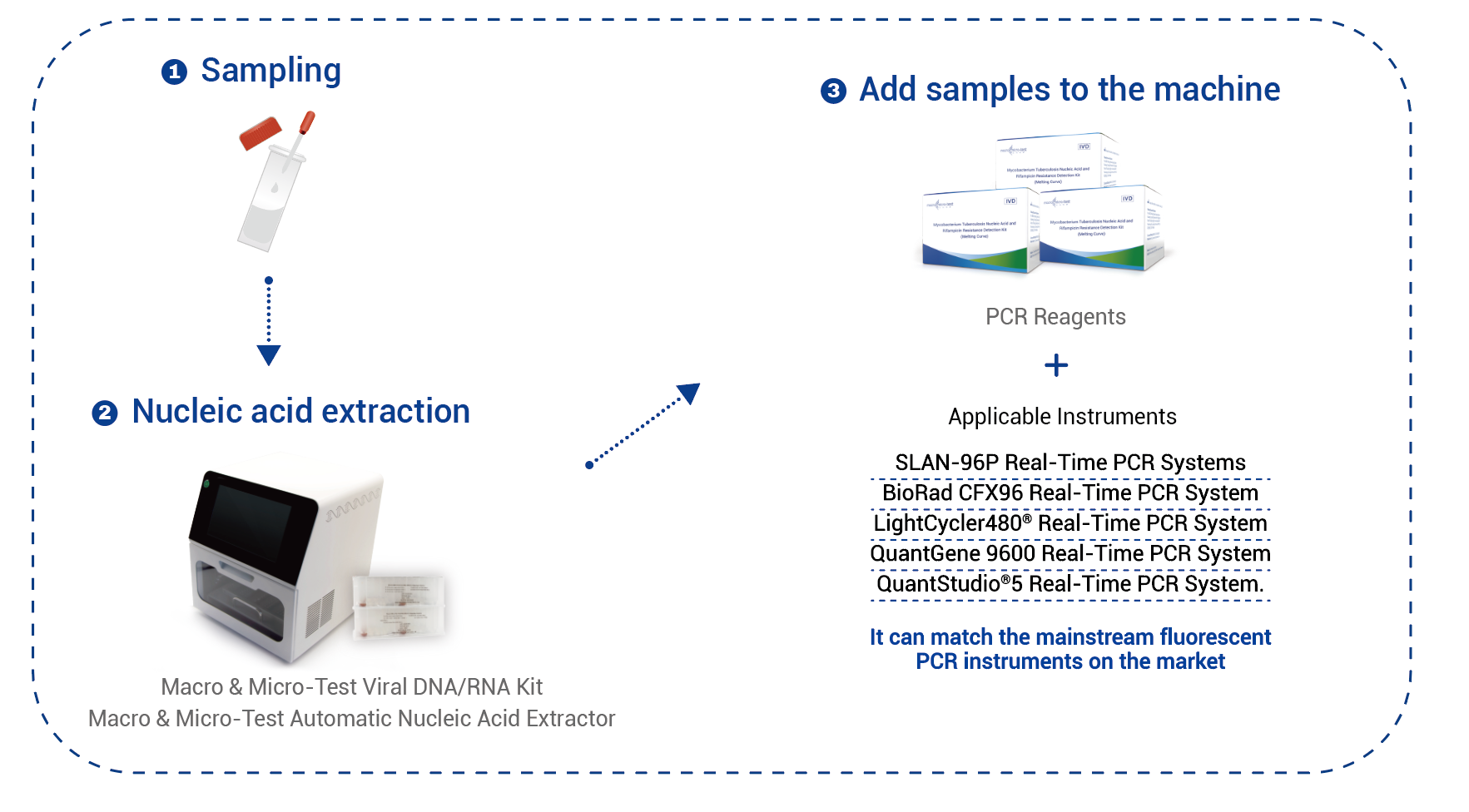
Se se emprega o kit xeral de ADN/ARN Macro & Micro-Test (HWTS-3019-50, HWTS-3019-32, HWTS-3019-48, HWTS-3019-96) (que se pode empregar co extractor automático de ácidos nucleicos Macro & Micro-Test (HWTS-3006C, HWTS-3006B)) ou a columna de ADN/ARN viral Macro & Micro-Test (HWTS-3022-50) de Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. para a extracción, engada 200 μL do control positivo, control negativo e mostra de esputo procesada que se vai analizar en secuencia e engada 10 μL do control interno por separado á mostra de control positivo, control negativo e mostra de esputo procesada que se vai analizar, e os pasos seguintes deben levarse a cabo estritamente segundo as instrucións de extracción. O volume de mostra extraída é de 200 μL e o volume de elución recomendado é de 100 μL.